Apesar de fazerem parte de praticamente tudo que utilizamos, os compostos químicos têm uma má reputação. Embora seja verdade que alguns compostos químicos sejam benéficos, todos eles podem ser perigosos sob certas condições.
Os itens dessa lista apresentam compostos químicos que são perigosos mesmo sob as condições normais de uso.
Ácido Fluorídrico

O ácido fluorídrico (HF) é um composto que deve ser utilizado com muito cuidado. O seu maior perigo é que, se em contato com a pele, ela não a queima, mas causa danos internos. Como não são vistos, muitas pessoas acabam deixando que ele aja. Seu modo de agir é entrando pela pele e atacando o cálcio dos ossos. Desse modo acaba por enfraquecer e até corroer parte do osso.
Sua aparência é de um líquido incolor e fumegante. Ele é muito utilizado na produção de criolita, gases refrigerantes, sais fluorados e defensivos agrícolas. Sua obtenção vem da reação entre o ácido sulfúrico e a fluorita seca. Pode ser usado também em sua forma líquida, na produção de diversos fármacos, como fluoxetina, ou Prozac.
A indústria petroquímica faz uso de ele tanto em estado gasoso quanto em solução. Ele é usado para a composição de muitos superácidos, como o trifluorometanosulfónico (CF3SO3H) ou o Ácido Fluorossulfúrico (FSO3H). Ele é usado também em grande quantidade na fusão e na refinação de alumínio secundário, e pode ser usado na indústria de vidros como um agente para a corrosão do mesmo, criando o efeito do jato de areia e de vidro fosco.
Trifluoreto de cloro
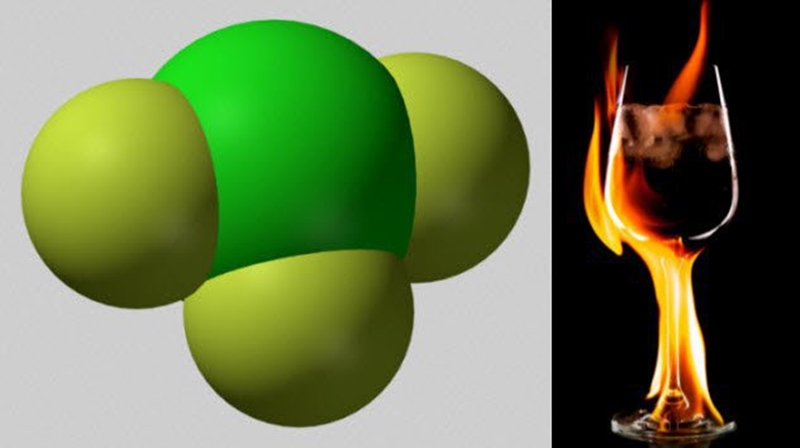
O Trifluoreto de Cloro é um composto muito famoso, conhecido como “agente florante”. Agentes fluorantes rompem as moléculas e trocam seus átomos de hidrogênio por flúor, o resultado é o que os químicos chamam de “reação exotérmica violenta”, ou como mais comumente chamado, Fogo de Flúor. É mais perigoso do que o gás de flúor, um gás que por si só já é perigoso.
Ele é, também, um agente oxidante melhor que o próprio oxigênio. Agentes oxidantes são compostos que tomam para si elétrons de outros compostos em uma reação, e isso é o que faz com que a combustão aconteça. Trifluoreto de Cloro é tão bom como oxidante, que ele pode queimar coisas que ninguém considera inflamável, tais como: tijolos, amianto ou até mesmo coisas que já queimaram antes.
Durante o início dos anos 50, na primeira tentativa de transporte de Trifluoreto de Cloro, o tanque de aço que o levava rachou e uma tonelada inteira do composto vazou. Ele queimou a temperaturas tão altas que não só acabou com todo o concreto da estrada, como também queimou um metro de cascalho e terra abaixo do concreto. Uma testemunha que presenciou o acidente o descreveu apenas com a frase: “O concreto… estava em chamas!”
Trifluoreto de Cloro ainda é fabricado e é usado por empresas de semicondutores para limpar seus equipamentos.
Dimetil mercúrio

Dimetil mercúrio (também escrito como dimetilmercúrio) é um composto químico organometálico de fórmula ((CH3)2Hg). É um líquido incolor, inflamável, e uma das mais potentes neurotoxinas conhecidas. É descrito como tendo um sabor levemente doce, embora a inalação do seu vapor, suficiente para chegar a essa conclusão, implicaria significativa exposição ao produto químico, o que pode ser perigoso. É extremamente perigoso. Até mesmo uma dose pequena, como 0,001 mL, podem ser fatais. Os riscos são agravados dada a alta pressão de vapor do líquido.
Dimetil mercúrio atravessa barreiras do látex, PVC, butyl, e neoprene rapidamente (em segundos) e é absorvido pela pele. Portanto, a maioria das luvas utilizadas em laboratório não fornece proteção adequada para ele. A única maneira segura para lidar com dimetil mercúrio é utilizando luvas laminadas de alta resistência debaixo de luvas pesadas revestidas de neoprene. Outros equipamentos de segurança são necessários, como um escudo sobre o rosto.
Esse composto pode atravessar a barreira hemato-encefálica com facilidade, provavelmente devido à formação de um complexo com a cisteína. É eliminado do organismo lentamente, e, portanto, tende a se acumular no organismo. Os sintomas do envenenamento podem demorar meses para aparecerem, o que, possivelmente, faria com que o tratamento não tivesse sucesso.
A toxicidade desse composto teve destaque com a morte do químico inorgânico Karen Wetterhahn do Dartmouth College, em 1997, meses após o derramamento de não mais do que algumas gotas do composto em sua mão, que estavam protegidas com luvas de látex.
Cianeto de potássio
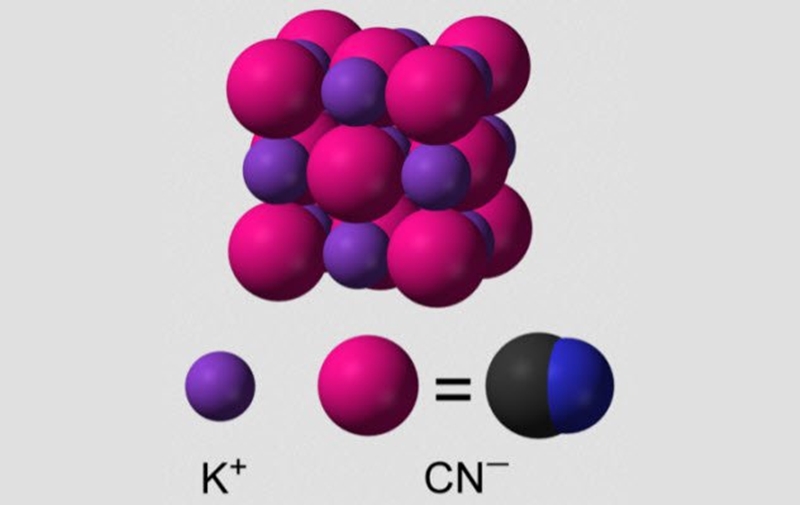
Cianeto de Potássio ou Cianureto de potássio é um composto químico altamente tóxico. Na verdade, é o íon cianeto (CN) que causa a intoxicação, pois ao ser absorvido pelo corpo humano gera a Citocromo c oxidase, uma enzima que impede a respiração celular, o que, por sua vez, faz com que o indivíduo tenha uma morte rápida. Soldados alemães capturados na Segunda Guerra Mundial, utilizavam esse composto para cometer suicídio através de ingestão. O mesmo foi utilizado, também, no suicídio coletivo de Jonestown.
Deve-se tomar o máximo de cuidado ao manipula-lo, já que o contato com qualquer ácido pode converte-lo em ácido cianídrico (HCN), um composto letal. Tanto o cianeto de potássio quanto o ácido cianídrico são considerados compostos hemotóxicos (que intoxicam o sangue). O ácido cianídrico foi, inclusive, utilizado como arma química pelos alemães, além de cloro gasoso e fosgênio.
Difluoreto de dioxigénio
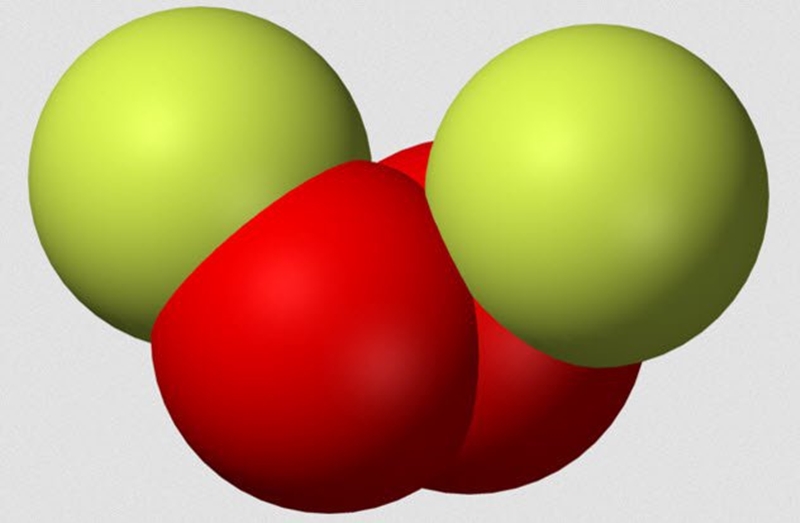
Difluoreto de dioxigénio é um produto químico muito perigo que, curiosamente, atende pelo apelido de FOOF, pois leva em sua fórmula dois átomos de flúor e dois átomos de oxigênio. Em 1962, o químico A.G. Streng publicou um livro chamado “As propriedades químicas de Dioxygen Difluoride.” Embora o título não seja muito empolgante, as experiências relatadas por Streng certamente foram. FOOF só pode ser obtido a temperaturas muito baixas, pois só entra em ebulição por volta dos -57°C.
Durante seus experimentos, Streng relatou que FOOF explodiu ao entrar em contato com compostos orgânicos, mesmo a -183°C. Se misturado ao Cloro, FOOF causa uma explosão muito violenta. Efeito semelhante ocorre se entrar em contato com a platina. O artigo de Streng é cheio de expressões do tipo “explosão”, “violenta”, “chamas” e “faísca”, o que serve para alertar sobre o grau de perigo desse composto.




